cellZscope™
細胞タイトジャンクションリアルタイムモニタリングシステム


cellZscope™は生理学的な状態の下で細胞層の経上皮/内皮電気抵抗値を自動測定する装置です。
コンピューター制御により長時間のモニタリングを、同時に24ウェルまで可能にしました。
インサートメンブレン上で様々なタイプの細胞を培養し、そのバリア機能(タイトジャンクション)形成を評価できます。
細胞層のオーム抵抗(TER; 経上皮/内皮抵抗値)及びキャパシタンス(Ccl)を測定します。
特徴
-
- 細胞培養中に測定が可能
- 培地交換や薬剤添加が可能
- 各社のセルカルチャーインサートが使用可能
- それぞれの電極が独立
- 最大96サンプルまで同時測定可能
- 複数のインサートサイズを同時に測定可能
-
cellZscope™各モデルの詳細内容については、各ページをご覧ください。
アプリケーションノート
アプリケーション
- タイトジャンクション(TJ)形成過程の解析
-
-
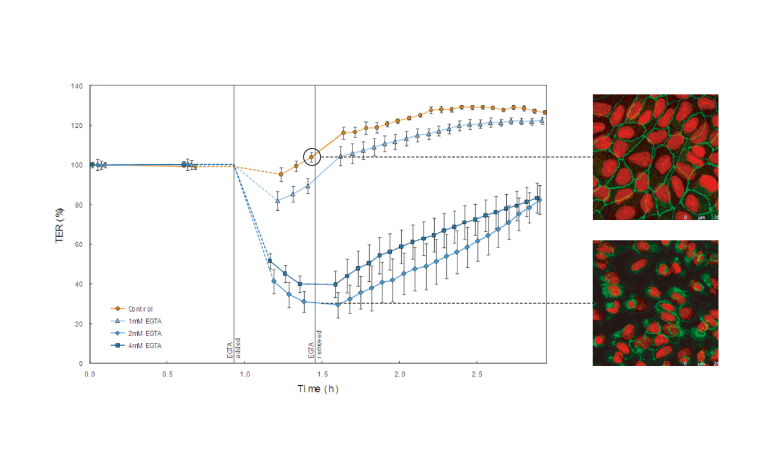
- EGTAはキレート作用によりCaイオンを枯渇させ細胞間のタイトジャンクション(TJ)を開口させます。ここではMDCK細胞をコンフルエントまで培養した後、EGTAを添加し、TERの変化を測定実施。続いて培地交換することでEGTAを除去すると、TERが上昇しTJが再形成されることが分かります。
- 画像はTJの裏打ちタンパク質であるZO-1の免疫染色による画像解析。画像からもTJが開口していることが確認できます。cellZscope™はラベルフリー且つ非侵襲にTJを解析するのに最適です。
-
-
- Methyl-beta-Cyclodextrin(MBCD)添加によるコレステロール枯渇時のモニタリング
-
-
- 濃度の異なるMBCDを各細胞の頂端側(apical side)に加え、MDCK細胞のTER値とキャパシタンス(Ccl)をモニタリング。
- MBCD添加直後に観察されるTER値の上昇はすでに様々な文献で取り上げられており、生化学的にも種々に説明されています[1,2]。
- TER値と同時に得られるキャパシタンスは、細胞層の他の特性が薬物量に応じて変化すること、具体的には細胞膜の形態変化を示しています。MBCD添加によるキャパシタンスの減少は共焦点顕微鏡での観察結果と一致しています[3]。
- 細胞膜のコレステロール枯渇は、microvilli(微絨毛)とmicroridges(隆起構造)の退縮をもたらします。細胞層の電気的なキャパシタンスは細胞膜の形態に影響を受ける為、薬物添加量の増加に伴いキャパシタンスが低下するのです。
- 今回はmicrovilliとmicroridgesの隆起の収縮が表面積の減少につながり、キャパシタンスが減少しました。cellZscope™を使用すればそのような細胞の微細な変化を一切見逃すことなく、細胞膜の変化を実験中、常に確認することができます。
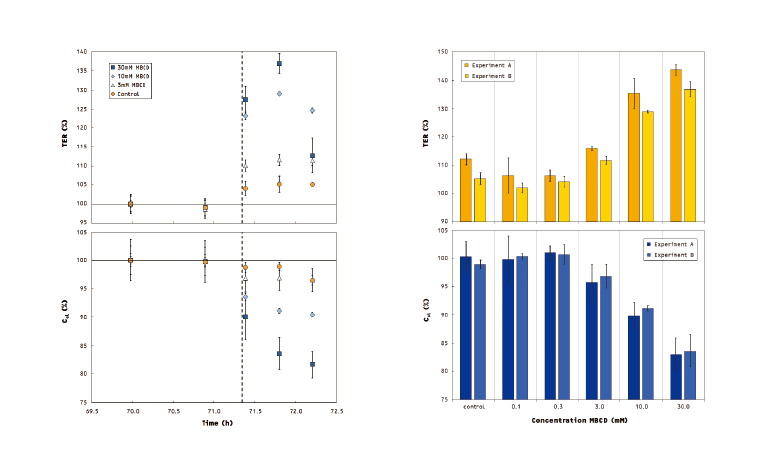
- MBCD添加(点線)に対し、MDCK-II細胞のTERとCcl値は添加量に依存して応答することが示された。データは3ウェルの平均値と標準偏差を示す(左図)。
- MBCD添加30分後、コレステロール減少によるMDCK-II細胞のTERとCclの測定結果(実験2回分)を示す(右図)。
[1]Stankewich, M., Francis, S.A., Vu, Q.U., Schneeberger, E.E., Lynch, R.D., Alterations in Cell Cholesterol Content Modulate Ca2+ -Induced Tight Junction Assembly by MDCK Cells. Lipids 31, 817 (1996).
[2]Francis, S.A., Kelly, J.M., McCormack, J., Rogers, R.A., Lai, J., Schneeberger, E.E., Lynch, R.D.: Rapid reduction of MDCK cellcholesterol by methyl-cholesterol by methyl-beta-cyclodextrin alters steady state transepithelial electrical resistance. Eur. J. Cell. Biol. 78 (1999).
[3]Colarusso, P., Spring, K.R.: Reticulated Lipid Probe Fluorescence Reveals MDCK Cell Apical Membrane Topography. Biophys. J. 82, 752 (2002).
-
-
- TER測定の比較_cellZscope™ vs. 手動型(チョップスティック型電極)
-
手動測定vs.自動測定
-
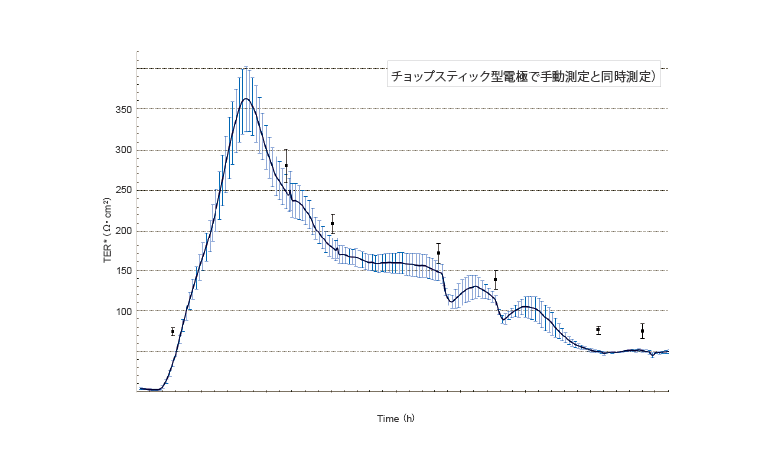
- cellZscope™内のインサートを手動のチョップスティック型電極で測定した場合(青色点)、cellZscope™で自動モニタリングした場合(青色曲線)、いずれにおいてもTERは同様の動きを見せた(培養22時間までは上昇し、以後下降トレンド。70時間を境に安定)。cellZscope™装置での連続測定データでは、チョップスティック型電極と比較して多くの詳細な変化をモニタリングすることができます。
- 2つの測定データを見ると、チョップスティック型電極でのTER値がやや高いことがわかります。これはチョップスティック型電極間では電解分布の不均一性の原因から、TER値を誤って高く測定する傾向があるためです[1]。
[1]Jovov, B., Wills, N.K., Lewis, S.A., A spectroscopic method for assessing confluence of epithelial cell cultures, Am. J. Physiol. Cell Physiol. 261, C1196 (1991).
-
インキュベータ内測定vs.クリーンベンチ測定
-
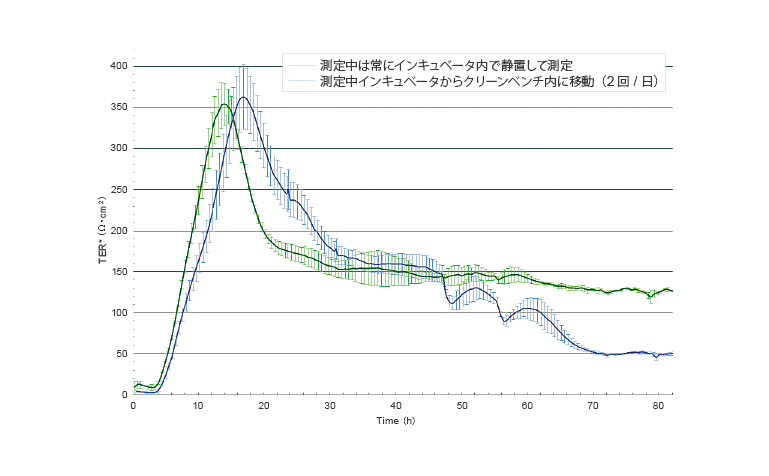
- 2台のcellZscope™、すなわち1台は常にインキュベータ内で静置して測定(緑色曲線)、もう1台はクリーンベンチ内へ数回移動させ、チョップスティック型電極を挿して測定(青色曲線)。得られた結果を比較すると、インキュベータ内で静置して培養した方が、経過時間に伴うTER値のはなめらかな曲線を示します。
- この事からインサートをインキュベータ外へ持ち出し、チョップスティック型電極を繰り返し挿入することがバリア形成細胞の障害になると考えられます。培養期間が長くなればなる程、TER値が極度に低下することになります。
- 細胞は外界の影響を受けずに安定した状況で培養することが望ましく、培養条件を均一に保つ事が欠かせません。cellZscope™システムは非侵襲の測定方式であり、人為的な影響を最小限に抑える画期的な装置です。
-
-
- 細胞の品質管理に
-
-
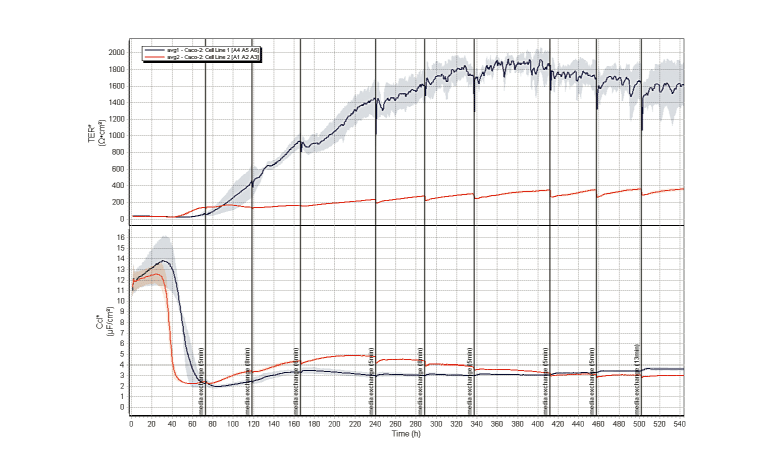
- 入手元の異なる2種類のCaco-2細胞のバリア特性を評価。バリア特性状況が全くことなることから細胞層の品質管理や薬物透過性試験直前の細胞層の状態の把握に大きな力を発揮します。
-
-
原理
- バリア形成組織
-
-
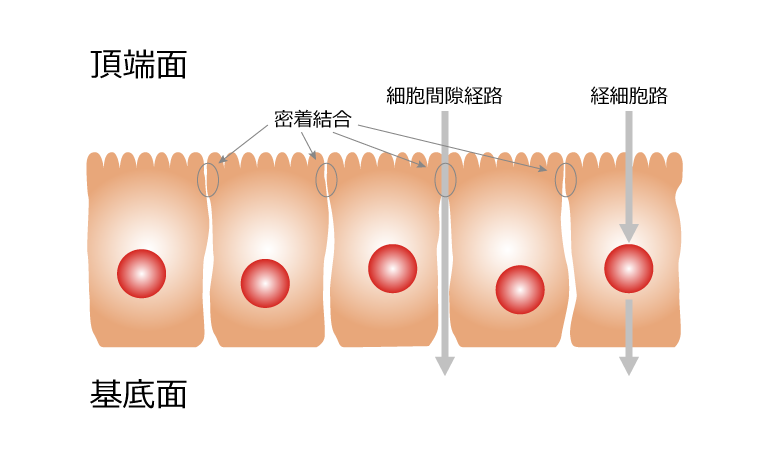
上皮及び内皮細胞層は選択的に分子を透過させるバリア機能を形成します。頂端面(apical side)から基底面(basolateral side)へ (そ の逆方向も同様に)の分子及びイオンの輸送には、経細胞路(transcellular route)、あるいはタイトジャンクションすなわち細胞間隙経路(paracellular route)が使われます。
上皮/ 内皮細胞バリアの主な構成要素は隣接した細胞間の密着結合(tight junction)です。
細胞内部及び外部からの様々なシグナルに応答しタイトジャンクションが選択的に開閉して分子の通過を調節しています。
細胞層の膜透過と電気抵抗、いわゆる経上皮/ 内皮電気抵抗値(TER)は直接的な相関性が見られます。「緊密な細胞層は高い電気抵抗値を示す」「高い透過性は低い電気抵抗値と関連がある」などの事実は、評価試験方法の基礎として現在活用されています。
従って、細胞層の電気抵抗を測定することはバリア形成組織を定量化する為には最適なパラメータです。これらの数値データを記録し、比較することで、細胞層バリアの形成や変化を測定することが可能になります。 -
-
- 細胞層のインピーダンス測定
-
-
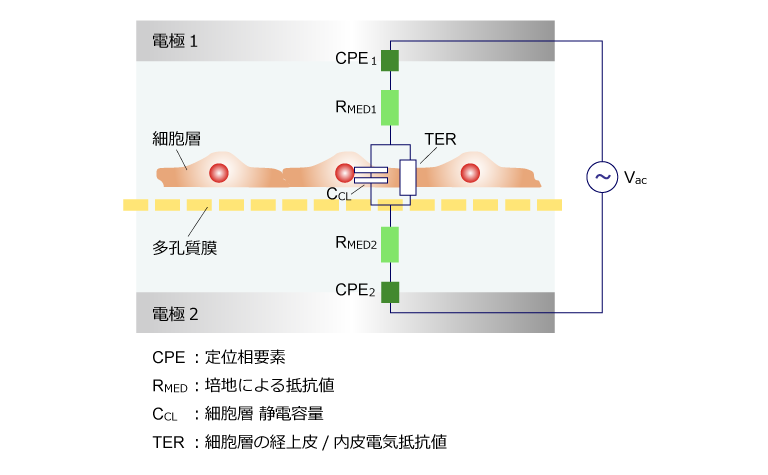
- インサート上に培養した細胞層を電気的に測定します。インサート膜の上下にそれぞれ電極を置いて微小交流電圧(Vac)を加え、インピーダンスを測定します。
- 細胞層の経上皮/内皮電気抵抗値(TER)およびキャパシタンス(静電容量、Ccl)は、周波数依存インピーダンス(Z)を等価回路で分析することによって測定します。
- 細胞層バリアに直接関連する2つの主なパラメータは抵抗値(TER)と静電容量(Ccl)です。オーム抵抗(TER)は細胞間隙短経路(paracellular route)を表します。一方頂端膜から基底膜を通る経細胞路(transcellular route)の静電容量はCclで要約されます。
-
-
- インピーダンススペクトル
-
- 細胞層のTERとCclは主に中間周波数域に表れ、水平状態を形成します。
- 水平状態が存在することでこれらTERとCclとその他周波数周辺(電極と培地の界面、及び培地成分)のインピーダンスを区別することができます。
測定方法
※YouTubeにてご覧いただけます。
セルカルチャーインサート
cellZscope™は市販セルカルチャーインサートをお使いいただけます。6ウェル用、12ウェル用、24ウェル用の3サイズをご用意しております。
詳しくは下記のセルカルチャーインサートページをご覧ください。
データ集・論文
デモ依頼・お問い合わせ
cellZscope™についてのよくあるご質問、お問い合わせ・デモ依頼は以下よりお願いいたします。